I. Overzicht van deESMORichtlijn 2025
In augustus 2025 publiceerde ESMO officieel de 'Early and locally advanced non small cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow up' in het toonaangevende oncologische tijdschrift Annals of Oncology. Dit is de eerste uitgebreide update sinds de versie uit 2017 en vormt een zeer gezaghebbende referentie voor oncologen wereldwijd.

Longkanker kent wereldwijd de hoogste incidentie en mortaliteit van alle kwaadaardige tumoren. Elk jaar zijn er meer dan 2,2 miljoen nieuwe gevallen en meer dan 1,8 miljoen sterfgevallen, waardoor longkanker de belangrijkste doodsoorzaak door kanker is bij zowel mannen als vrouwen. Niet-kleincellige longkanker (NSCLC) is verantwoordelijk voor ongeveer 80-85% van alle longkankerpatiënten. Tegen deze ernstige achtergrond geeft de publicatie van de richtlijn voor 2025 een nieuwe wetenschappelijke impuls aan de klinische praktijk, waarbij de update over strategieën voor biomarkeronderzoek bijzonder belangrijk is.
II. Interpretatie van belangrijke updates van de richtlijnen
2.1 Biomarkeronderzoek: van “optioneel” naar “essentieel”
De richtlijn van 2025 brengt een belangrijke strategische aanpassing met zich mee met betrekking tot biomarkeronderzoek. De richtlijn stelt expliciet dat biomarkeronderzoek essentieel is voor de behandelbeslissing bij patiënten met stadium IB-III NSCLC.
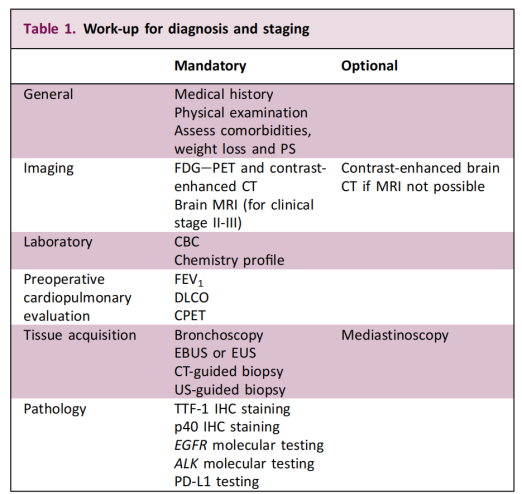
Deze aanbeveling breidt moleculaire diagnostiek uit van de eerdere focus op patiënten met een gevorderde ziekte naar gevallen in een vroeg stadium die operatief te behandelen zijn. Het belangrijkste doel is het identificeren van drijvende genmutaties en het bieden van een wetenschappelijke basis voor gepersonaliseerde precisiebehandeling. De richtlijn benadrukt tevens dat de haalbaarheid van een biopsie en de diagnostische aanpak moeten worden bepaald door een multidisciplinair team op basis van de kenmerken van de patiënt en de tumor.
Wat de specifieke teststrategie betreft, beveelt de richtlijn duidelijk aan dat genetische testen worden uitgevoerd vóórdat een chirurgische ingreep wordt overwogen, en dat deze testen in ieder geval EGFR en ALK moeten omvatten. Dit concept van "vooraf testen" heeft een grote klinische betekenis voor de precieze stratificatie en gepersonaliseerde behandeling van NSCLC in een vroeg stadium – de tijdigheid en nauwkeurigheid van de testresultaten bepalen direct de keuze voor de daaropvolgende adjuvante therapie.
2.2 Therapeutische doorbraken bij NSCLC in een vroeg stadium met positieve driver-oncogenen
De richtlijn voor 2025 integreert bewijs uit meerdere grote klinische studies om een duidelijk, nauwkeurig behandelingsplan op te stellen voor patiënten met NSCLC in een vroeg stadium die een driver-oncogen vertonen.
EGFR-gemuteerde positieve patiënten:Op basis van de baanbrekende ADAURA-studie is postoperatieve adjuvante osimertinib gedurende drie jaar de wereldwijde standaardbehandeling geworden voor patiënten met EGFR-exon 19-deleties of exon 21 L858R-mutaties. De ADAURA-studie is een internationale, multicentrische, gerandomiseerde, gecontroleerde fase III-studie die de werkzaamheid en veiligheid van adjuvante osimertinib evalueert bij patiënten met volledig gereseceerd stadium IB-IIIA EGFR-gemuteerd NSCLC. De studie toonde aan dat osimertinib de ziektevrije overleving en de algehele overleving significant verbeterde in vergelijking met placebo, waardoor osimertinib de nieuwe standaardbehandeling voor deze patiëntengroep werd. Verkennende analyses van de ADAURA-studie gaven echter aan dat ongeveer 36% van de vroegtijdige stopzettingen van de behandeling te wijten was aan bijwerkingen en nog eens 31% aan een beslissing van de patiënt. Deze bevinding benadrukt de noodzaak van nauwkeurige baseline-testen vóór de behandeling om ervoor te zorgen dat gerichte therapie wordt gegeven aan patiënten die er langdurig baat bij kunnen hebben.
ALK-positieve patiënten:Op basis van de ALINA-studie is postoperatieve adjuvante alectinib gedurende twee jaar nu de standaardbehandeling. In de primaire analyse van de gerandomiseerde, open-label fase III ALINA-studie toonde alectinib een significant voordeel in ziektevrije overleving bij patiënten met stadium II-IIIA, met een hazard ratio van 0,24. Bijgewerkte gegevens van de ALINA-studie, gepresenteerd op het ESMO 2025-congres, toonden aan dat na ≥3 jaar follow-up het voordeel van alectinib in ziektevrije overleving "aanhoudend en klinisch relevant" bleef, met een hazard ratio van 0,36 bij patiënten met stadium II-IIIA. De laatst gerapporteerde algehele overlevingskans na 4 jaar bedroeg 98,4%, de ziektevrije overleving na 4 jaar was 75,5%, en ook de ziektevrije overleving in het centrale zenuwstelsel was verbeterd, zonder nieuwe veiligheidssignalen. Deze robuuste gegevens bevestigen de standaardbehandeling met adjuvante alectinib na resectie van ALK-positief NSCLC en onderstrepen het belang van nauwkeurige diagnostiek om dergelijke patiënten te identificeren.
Keuze van de testmethode:De ESMO-richtlijn van 2025 vermeldt explicietmultiplex RT-PCR paneltestenNaast RNA-gebaseerde NGS, IHC en FISH wordt ALK-fusiedetectie aanbevolen als een van de technische methoden. Dit geeft aan dat de kernvereiste van de richtlijn is om testen uit te voeren ter ondersteuning van klinische beslissingen, in plaats van een specifiek testplatform voor te schrijven. Voor RT-PCR-producten gericht op EGFR- en ALK-detectie biedt deze flexibele teststrategie een sterke, op richtlijnen gebaseerde rechtvaardiging voor het gebruik ervan in de klinische praktijk.
III. Technische oplossingen voor precisietesten
De richtlijn van 2025 verplaatst de testen naar de fase vóór de chirurgische besluitvorming, wat de eisen aan nauwkeurigheid, gevoeligheid en toegankelijkheid van de tests verhoogt. De twee hieronder beschreven RT-PCR-gebaseerde detectieproducten voldoen technisch gezien precies aan de eisen van de richtlijn.
3.1 EGFR-mutatiedetectiekit – Verbeterd ARMS-technologieplatform
KerntechnologieDe verbeterde ARMS-technologie maakt specifieke amplificatie mogelijk van mutante sequenties met een lage abundantie tegen een hoge wildtype-achtergrond.
Drie technische beveiligingsmaatregelen:
-Verbeterde ARMS → verbetert de herkenning van mutaties
-Enzymatische verrijking → verteert de wildtype-achtergrond en verrijkt de mutante sequenties
-Temperatuurblokkering → onderdrukt niet-specifieke amplificatie
Prestatie: Gevoeligheid van1% mutante allelfrequentie
BesmettingsbeheersingIngebouwde interne controle + UNG-enzym voorkomen besmetting.
Doorlooptijd: Werking met gesloten buis, ongeveer120 minuten
Voorbeeldcompatibiliteit:Weefsel/vloeibare biopsiemonsters → voldoet aan de eis van "vooraf testen"
Dekking:45 mutatiesin EGFR-exonen 18-21, precies overeenkomend met de in de richtlijnen gemarkeerde regio's (deleties in exon 19 en L858R in exon 21)
Klinisch gebruik: Geeft direct richting aan EGFR-TKI-therapie
3.2 MMT EML4-ALK Fusion Detection Kit – RNA-gebaseerde oplossing voor fusiedetectie

-TechnologieplatformRNA-gebaseerde RT-PCR biedt inherente voordelen ten opzichte van DNA-gebaseerde methoden voor fusiedetectie.
-RNA-gebaseerd voordeelDetecteert direct tot expressie gebrachte fusietranscripten, waardoor vals-negatieve resultaten effectief worden vermeden.
-Bewijs uit de studieBij ALK-fusies met een lage abundantie is RT-PCR aanzienlijk betrouwbaarder dan DNA-gebaseerde tests.
-GevoeligheidDetecteert fusies tot20 kopieën per reactie
-Dekking van variantenOmslagen12 veelvoorkomende EML4-ALK-fusievarianten(inclusief variant 1 ~33%; varianten 3a/3b samen ~29%)
-Bedrijfsvoering en verontreinigingsbeheersingGesloten buis, circa 120 minuten; ingebouwde procescontroles + UNG-enzym voorkomen valse resultaten.
-InstrumentcompatibiliteitCompatibel met diverse gangbare real-time PCR-instrumenten.
-Afstemming van richtlijnen: Zeer consistent met de ESMO-richtlijn
IV. Overeenstemming tussen de tests en de aanbevelingen in de richtlijnen
De twee detectieproducten komen in de volgende belangrijke aspecten sterk overeen met de ESMO 2025-richtlijn voor vroegtijdig en lokaal gevorderd niet-kleincellig longkanker:
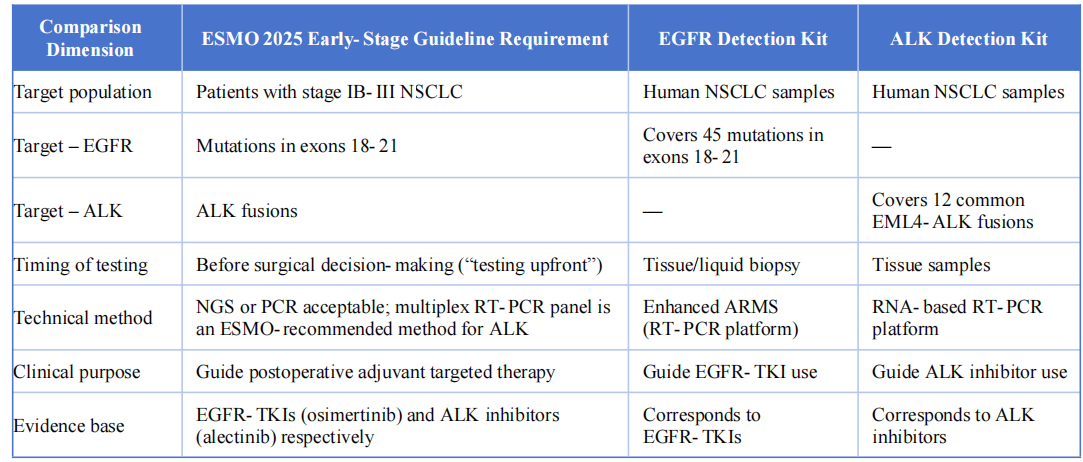
V. Conclusie
De ESMO 2025-richtlijn voor niet-kleincellige longkanker in een vroeg stadium luidt een nieuw tijdperk in van precieze diagnose en behandeling, gericht op “Voorafgaande tests, nauwkeurige targeting en optimalisatie van de behandeling."De EGFR-mutatiedetectiekit en de MMT EML4-ALK-fusiedetectiekit voldoen aan de eisen van de richtlijn voor targets, timing en nauwkeurigheid via verschillende technische trajecten."
De EGFR-kit maakt gebruik van verbeterde ARMS-technologie voor zeer gevoelige detectie van gerichte mutaties in beperkte monsters, en ondersteunt zowel weefsel- als vloeistofbiopsie om "vooraf testen" mogelijk te maken.
De ALK-kit is gebaseerd op RNA-gebaseerde RT-PCR en biedt voordelen ten opzichte van DNA-methoden voor fusiedetectie, wat aansluit bij de aanbeveling van ESMO voor multiplex RT-PCR-panels voor ALK-testen.
Samen vormen deze twee producten een nauwkeurige testoplossing die voldoet aan de ESMO 2025-richtlijn en die gepersonaliseerde adjuvante therapie voor NSCLC in een vroeg stadium ondersteunt.
Referenties:
- Zer A, Ahn MJ, Barlesi F, et al. Vroege en lokaal gevorderde niet-kleincellige longkanker: ESMO Klinische Praktijkrichtlijn voor diagnose, behandeling en follow-up. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Geplaatst op: 6 mei 2026

