Mycobacterium tuberculosis nucleïnezuur en rifampicineresistentie
Productnaam
HWTS-RT074B-Mycobacterium Tuberculosis Nucleïnezuur- en Rifampicineresistentie Detectiekit (Smeltcurve)
Certificaat
CE
Epidemiologie
Mycobacterium tuberculosis, kortweg tuberculosebacil of TB, is de pathogene bacterie die tuberculose veroorzaakt. De meest gebruikte eerstelijnsgeneesmiddelen tegen tuberculose zijn onder andere isoniazide, rifampicine en hexambutol. Tweedelijnsgeneesmiddelen zijn onder andere fluoroquinolonen, amikacine en kanamycine. Nieuwe geneesmiddelen die ontwikkeld zijn, zijn linezolid, bedaquiline en delamani. Door onjuist gebruik van deze geneesmiddelen en de specifieke structuur van de celwand van Mycobacterium tuberculosis ontwikkelt deze bacterie echter resistentie tegen deze geneesmiddelen. Dit vormt een ernstige uitdaging voor de preventie en behandeling van tuberculose.
Rifampicine wordt sinds eind jaren zeventig veelvuldig gebruikt bij de behandeling van longtuberculosepatiënten en heeft een significant effect. Het is de eerste keus om de chemotherapie bij longtuberculosepatiënten te verkorten. Resistentie tegen rifampicine wordt voornamelijk veroorzaakt door een mutatie in het rpoB-gen. Hoewel er constant nieuwe antituberculosemiddelen op de markt komen en de klinische werkzaamheid bij longtuberculosepatiënten voortdurend verbetert, is er nog steeds een relatief tekort aan antituberculosemiddelen en komt irrationeel medicijngebruik in de klinische praktijk relatief vaak voor. Het is duidelijk dat de Mycobacterium tuberculosis bij longtuberculosepatiënten niet volledig en tijdig kan worden gedood, wat uiteindelijk leidt tot verschillende graden van resistentie tegen medicijnen in het lichaam van de patiënt, waardoor het ziekteverloop wordt verlengd en het risico op overlijden toeneemt.
Kanaal
| Kanaal | Kanalen en fluoroforen | Reactiebuffer A | Reactiebuffer B | Reactiebuffer C |
| FAM-kanaal | Verslaggever: FAM, Uitbuiter: Geen | rpoB 507-514 | rpoB 513-520 | 38KD en IS6110 |
| CY5-kanaal | Rapporteur: CY5, Blusser: Geen | rpoB 520-527 | rpoB 527-533 | / |
| HEX (VIC) kanaal | Verslaggever: HEX (VIC), Blusser: Geen | Interne controle | Interne controle | Interne controle |
Technische parameters
| Opslag | ≤-18℃ In het donker |
| Houdbaarheid | 12 maanden |
| Exemplaartype | Sputum |
| CV | ≤5,0% |
| LoD | Mycobacterium tuberculosis 50 bacteriën/ml rifampicine-resistente wildtype: 2x103bacteriën/ml homozygote mutant: 2x103bacteriën/ml |
| Specificiteit | Het detecteert wildtype Mycobacterium tuberculosis en de mutatieplaatsen van andere genen voor geneesmiddelresistentie, zoals katG 315G>C\A en InhA-15C>T. De testresultaten tonen geen resistentie tegen rifampicine aan, wat betekent dat er geen kruisreactiviteit is. |
| Toepasselijke instrumenten: | SLAN-96P Real-Time PCR-systemen BioRad CFX96 Real-Time PCR-systeem LightCycler480® Real-Time PCR-systeem |
Werkstroom
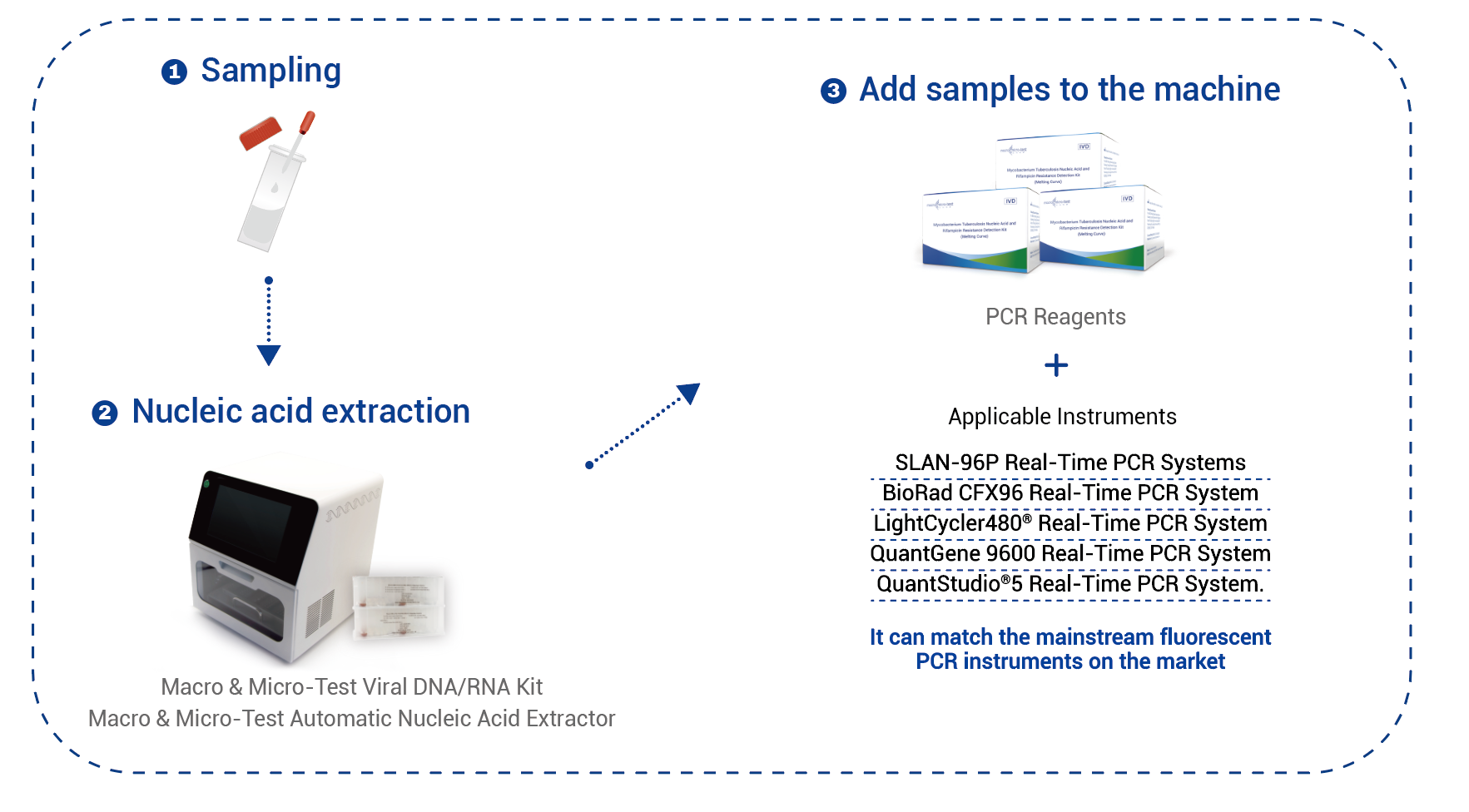
Als u de Macro & Micro-Test General DNA/RNA Kit (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (die gebruikt kan worden met de Macro & Micro-Test Automatic Nucleic Acid Extractor (HWTS-3006C, HWTS-3006B)) of de Macro & Micro-Test Viral DNA/RNA Column (HWTS-3022-50) van Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. gebruikt voor de extractie, voeg dan achtereenvolgens 200 μL van de positieve controle, de negatieve controle en het te testen bewerkte sputummonster toe. Voeg vervolgens afzonderlijk 10 μL van de interne controle toe aan de positieve controle, de negatieve controle en het te testen bewerkte sputummonster. De daaropvolgende stappen dienen strikt volgens de extractie-instructies te worden uitgevoerd. Het geëxtraheerde monstervolume bedraagt 200 μL en het aanbevolen elutievolume is 100 μL.