1. Achtergrond van de dengue-epidemie: een escalerende wereldwijde uitdaging voor de volksgezondheid.
Dengue is een acute, door muggen overgedragen virale ziekte die wordt veroorzaakt door het denguevirus (DENV). Het is uitgegroeid tot de snelst verspreidende arbovirale ziekte ter wereld en vormt een aanzienlijke bedreiging voor de volksgezondheid. De afgelopen twee decennia is de wereldwijde incidentie van dengue dramatisch toegenomen, waarbij het aantal gerapporteerde gevallen sinds 2021 jaarlijks is verdubbeld [1]. In december 2023 riep de Wereldgezondheidsorganisatie (WHO) een wereldwijde dengue-noodtoestand uit om de gecoördineerde internationale respons te versterken. Epidemiologische schattingen van de WHO geven aan dat ongeveer 3,9 miljard mensen wereldwijd risico lopen op een dengue-infectie, met naar schatting 390 miljoen infecties per jaar, waarvan 96 miljoen zich manifesteren als klinisch manifeste gevallen [1,2].
2 Epidemiologische hoogtepunten
De epidemiologische kenmerken van dengue worden bepaald door de interactie van virologische factoren, de ecologie van de vector, de immuunreactie van de gastheer en sociaal-omgevingsfactoren. Een grondig begrip van deze kenmerken is essentieel voor de ontwikkeling van effectieve preventie- en bestrijdingsstrategieën, evenals nauwkeurige diagnostische methoden.
2.1 Transmissievectoren en stedelijke transmissiepatronen
Het denguevirus wordt voornamelijk overgedragen doorAedes aegypti en Aedes albopictusmuggen. Van deze vectorsoorten wordt Aedes aegypti erkend als de belangrijkste transmissievector, gekenmerkt door een hoog "menselijk aanpassingsvermogen" en een wijdverspreide aanwezigheid in tropische en subtropische stedelijke omgevingen. In tegenstelling tot andere muggenvectoren van arbovirale pathogenen, vertoont Aedes aegypti de volgende belangrijke epidemiologische kenmerken:
-Een voorkeur voor voortplanting in door de mens beïnvloede omgevingen (bijv. wateropslagcontainers, afgedankte banden)
-Een sterke voorkeur voor menselijk bloed als voedingsbron
-Voedingsgedrag overdag
Deze kenmerken definiëren dengue als een typische ziekte“stedelijke infectieziekte,”waarbij de transmissie-efficiëntie aanzienlijk hoger ligt in dichtbevolkte gebieden. Studies van de WHO hebben aangetoond dat in dichtbevolkte stedelijke gebieden de toegenomen frequentie van contact tussen muggen en mensen het basisreproductiegetal (R₀) van DENV aanzienlijk kan verhogen, waardoor de verspreiding van epidemieën wordt versneld [2].
2.2 Wereldwijde verspreidingstrends en drijvende factoren
Volgens rapporten van de WHO is het wereldwijde aantal gemelde denguegevallen de afgelopen twee decennia exponentieel toegenomen [1,3]. Deze stijgende trend wordt voornamelijk veroorzaakt door de volgende onderling samenhangende factoren:
(1) Klimaatverandering: Stijgende wereldtemperaturen vergroten niet alleen het geografische verspreidingsgebied van geschikte habitats voor muggen die dengue overbrengen, maar verkorten ook de extrinsieke incubatietijd van DENV in de mug, waardoor de transmissie-efficiëntie toeneemt. Klimaatgerelateerde variaties in de muggendichtheid zijn door de WHO gevalideerd als een betrouwbare voorspeller van de ruimtelijke en temporele dynamiek van dengue-uitbraken.
(2) Verstedelijking: Snelle en ongeplande stedelijke uitbreiding heeft gezorgd voor overvloedige broedplaatsen voor muggen die het virus overbrengen, terwijl de toegenomen bevolkingsdichtheid de continuïteit van de DENV-transmissieketens heeft versterkt.
(3) Mondiale bevolkingsbewegingen: Internationaal reizen en handel hebben de snelle grensoverschrijdende verspreiding van DENV vergemakkelijkt, waardoor de overgang van geïmporteerde gevallen naar aanhoudende lokale verspreiding is bevorderd. Uit surveillancegegevens van de WHO blijkt dat de Verenigde Staten tussen 2010 en 2021 7.528 reisgerelateerde denguegevallen hebben gemeld, waarvan 3.135 ziekenhuisopname vereisten en 19 tot de dood leidden.
(4) Uitbreiding van de verspreiding van de vector: Wereldwijd blijft het geografische verspreidingsgebied van Aedes aegypti en Aedes albopictus zich uitbreiden, waarbij Aedes-muggen zich steeds meer vestigen in delen van Europa. Als gevolg hiervan is dengue geëvolueerd van een traditioneel regionale epidemie tot een wereldwijde bedreiging voor de volksgezondheid.
2.3 Mechanismen voor gelijktijdige circulatie van meerdere serotypen en herinfectie
Het denguevirus bestaat uit vier antigenetisch verschillende serotypen (DENV-1 tot en met DENV-4). Infectie met één serotype biedt langdurige beschermende immuniteit tegen dat specifieke serotype, maar slechts tijdelijke en gedeeltelijke kruisbescherming tegen de andere drie serotypen. De algemene bevolking is universeel vatbaar voor DENV, waarbij slechts een deel van de geïnfecteerde personen klinische ziekteverschijnselen ontwikkelt [2].
In endemische gebieden circuleren vaak meerdere DENV-serotypes tegelijk, waardoor individuen potentieel meerdere dengue-infecties gedurende hun leven kunnen oplopen. Epidemiologische studies van de WHO hebben aangetoond dat de gelijktijdige circulatie van meerdere serotypes een belangrijke oorzaak is van periodieke dengue-uitbraken [1].
2.4 Secundaire infectie en antilichaam-afhankelijke versterking
Een cruciaal en uniek fenomeen in de dengue-epidemiologie isantilichaam-afhankelijke versterking (ADE)Tijdens een secundaire infectie met een heteroloog DENV-serotype vergemakkelijken niet-neutraliserende antilichamen die tijdens de primaire infectie zijn geproduceerd de virale toegang tot monocyten en macrofagen, waardoor de virale replicatie wordt versterkt. Dit mechanisme wordt door de WHO algemeen erkend als een belangrijke pathogene factor bij ernstige dengue, waaronder dengue hemorragische koorts en dengue shocksyndroom [1].
Uit epidemiologische gegevens van de WHO blijkt steevast dat personen met een secundaire dengue-infectie een significant hoger risico lopen op het ontwikkelen van een ernstige vorm van de ziekte dan personen met een primaire infectie – een kenmerk dat van groot belang is voor ziektebewaking en klinisch management. Het is belangrijk om te benadrukken dat, hoewel het risico op een ernstige vorm van de ziekte verhoogd is tijdens een secundaire infectie, een infectie met elk DENV-serotype potentieel kan leiden tot ernstige dengue [1].
2.5 Niet-specifieke klinische verschijnselen en risico op verkeerde diagnose
De klinische verschijnselen van dengue zijn opvallend aspecifiek, vooral in de beginfase van de ziekte, en overlappen vaak met die van andere door muggen overgedragen virale infecties (bijvoorbeeld chikungunya- en zikavirussen) en bepaalde luchtweginfecties. Volgens schattingen van de WHO verloopt 40-80% van de DENV-infecties asymptomatisch [3].
Typische klinische verschijnselen zijn onder meer:
-Acute koorts (die 2-7 dagen aanhoudt en mogelijk in twee fasen verloopt)
-Ernstige hoofdpijn en retro-orbitale pijn (pijn achter de ogen)
-Spier- en gewrichtspijn (ook wel bekend als "knokkelkoorts")
-Maculaire of maculopapulaire uitslag
-Milde bloedingen (bijv. blauwe plekken, neusbloedingen, bloedend tandvlees)
Symptomatische dengue wordt doorgaans onderverdeeld in drie verschillende fasen: de koortsfase, de kritieke fase en de herstelfase. Ongeveer minder dan 5% van de symptomatische patiënten ontwikkelt zich tot ernstige dengue. Door het ontbreken van specifieke klinische kenmerken is een diagnose uitsluitend op basis van klinische symptomen lastig, wat het risico op een verkeerde diagnose of onderdiagnose vergroot. De WHO benadrukt expliciet dat een klinische diagnose alleen onvoldoende is om nauwkeurigheid te garanderen, waardoor laboratoriumbevestiging onmisbaar is [1].
3 belangrijke punten uit het WHO-rapport "Laboratoriumtesten voor het denguevirus: voorlopige richtlijnen, april 2025"
In april 2025 publiceerde de Wereldgezondheidsorganisatie (WHO) bijgewerkte tussentijdse richtlijnen voor laboratoriumtests op denguevirus (DENV). Deze richtlijnen bieden gezaghebbende technische richtlijnen voor de wereldwijde diagnose van dengue. Ze synthetiseren de meest recente inzichten in laboratoriumtests voor dengue in de context van de aanhoudende wereldwijde dengue-noodsituatie en bieden praktische aanbevelingen die zijn afgestemd op omgevingen met verschillende beschikbare middelen.

3.1 Fundamentele principes van teststrategie
De richtlijn benadrukt dat de diagnose van dengue een gecombineerde teststrategie met meerdere markers moet omvatten, gebaseerd op het stadium van de ziekte [1]. Gezien het ontbreken van een universeel diagnostisch algoritme, moeten teststrategieën worden aangepast aan de lokale epidemiologische context, waarbij rekening wordt gehouden met de volgende belangrijke factoren [1]:
- Infectiestadium: Het aantal dagen na het begin van de symptomen bepaalt welke testmethode het meest geschikt is.
-Monstertype: De geschiktheid van volbloed, plasma of serum voor DENV-detectie
-Regionale epidemiologie: De lokaal circulerende DENV-serotypes en de gelijktijdige circulatie van andere arbovirussen
- Risico op co-infectie: In regio's waar arbovirussen in meerdere gevallen circuleren, moet multiplex-testen worden overwogen om onderscheid te maken tussen verschillende ziekteverwekkers.
3.2 Fasegebaseerde teststrategie
Volgens de richtlijnen van de WHO moet het testen van dengue in het laboratorium duidelijke tijdsvensters volgen, gebaseerd op het stadium van de ziekte [1,2]:
(1) Testen in de acute fase (≤7 dagen na aanvang)
-Nucleïnezuurtesten (moleculaire testen): Reverse transcriptie-polymerasekettingreactie (RT-PCR) en andere moleculaire methoden detecteren DENV-RNA met een hoge gevoeligheid.
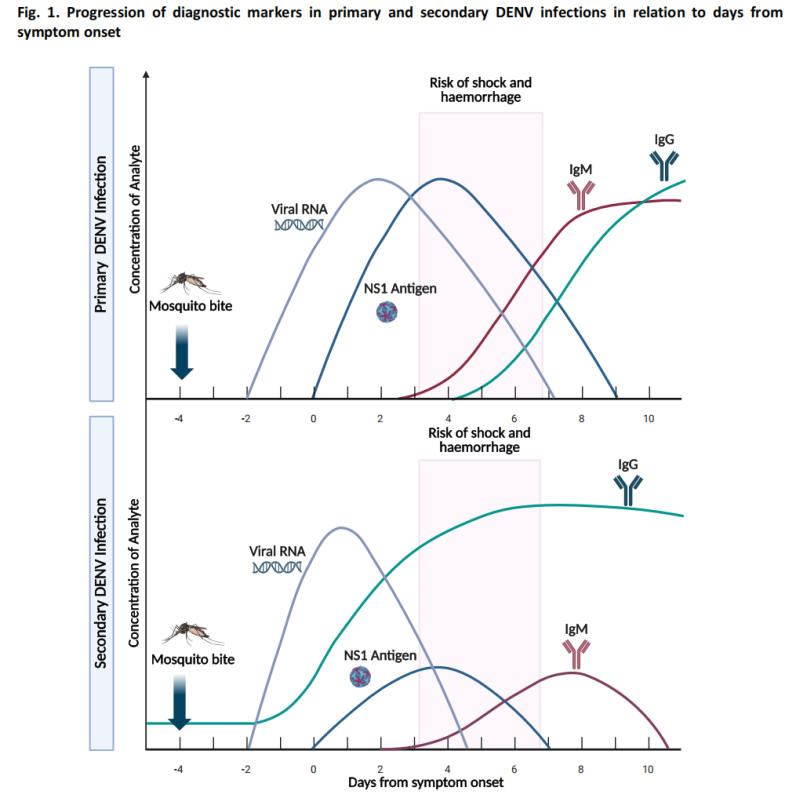
-Antigeentest: detectie van het NS1-antigeen, dat binnen 1-3 dagen na het begin van de symptomen aantoonbaar wordt.
Tijdens de acute fase zijn de virusniveaus relatief hoog en bereiken nucleïnezuur- en antigeentesten een optimale gevoeligheid.
(2) Testen tijdens de herstelfase (≥4 dagen na aanvang)
-Serologisch onderzoek: IgM-antilichamen worden doorgaans aantoonbaar rond dag 4 na het begin van de symptomen.
In de meeste gevallen blijven IgM-antilichamen 14 tot 20 dagen aanwezig, en in sommige gevallen kan dit oplopen tot 90 dagen.
-IgG-testen hebben beperkte waarde voor de diagnose van acute dengue vanwege mogelijke kruisreactieve antilichamen als gevolg van een eerdere flavivirusinfectie of vaccinatie.
(3) Diagnostisch algoritme voor verdachte gevallen
De richtlijnen omvatten een diagnostisch algoritme voor vermoedelijke denguegevallen, met aanbevelingen voor geschikte testmethoden op basis van het aantal dagen na het begin van de symptomen: NS1-antigeentesten en nucleïnezuurtesten zijn de belangrijkste benaderingen in de vroege fase, terwijl serologische testen de belangrijkste methode zijn in de latere fase.
3.3 Evaluatie en selectie van de prestaties van de testmethode
Volgens de WHO is een systematische evaluatie van de prestaties en toepassingsscenario's van verschillende dengue-tests als volgt:
| Testmethode | Doel | Tijdsvenster | Primair toepassingsscenario | Overwegingen |
| Nucleïnezuurtesten | Viraal RNA | 1-7 dagen na aanvang van de symptomen | Vroege bevestiging, serotype-identificatie | Gouden standaardmethode; vereist gespecialiseerde laboratoriumapparatuur en technische expertise. |
| NS1-antigeentest | Niet-structureel eiwit | 1-3 dagen na aanvang van de symptomen | Vroege snelle screening | Beschikbaar in de vorm van een snelle diagnostische test (RDT), geschikt voor omgevingen met beperkte middelen. |
| IgM-antilichaamtest | Specifieke IgM-antilichamen | ≥4 dagen na aanvang van de symptomen | Diagnose van een recente infectie | Een enkel serummonster wijst slechts op een mogelijke recente infectie; seroconversie is nodig voor bevestiging. |
| IgG-antilichaamtest | Specifieke IgG-antilichamen | Herstellende/eerdere infectie | Epidemiologisch onderzoek, beoordeling van de immuniteitsstatus | Een enkel serummonster is niet geschikt voor de diagnose van acute dengue. |
| Gecombineerde testen (NS1+IgM/IgG) | Antigeen + antilichamen | Volledig ziekteverloop | Uitgebreide diagnose van dengue-infectie | Momenteel het best presterende RDT-formaat voor de diagnose van dengue. |
| NGS | Viraal RNA | 1-7 dagen na aanvang van de symptomen | Virale genoombewaking | Vereist gespecialiseerde sequentiebepalingsapparatuur en bio-informatische analysemogelijkheden. |
4 macro- en microtests: productaanbevelingen voor dengue-detectie per scenario.
Om de preventie en bestrijding van dengue te ondersteunen, biedt Macro & Micro-Test een geïntegreerd diagnostisch portfolio dat snelle screening, moleculaire bevestiging en genomische surveillance omvat, en dat voldoet aan de behoeften in de verschillende fasen van de bestrijding van uitbraken.
4.1 Scenario 1: Snelle screening en gerichte surveillance
Van toepassing op koortsklinieken, eerstelijnszorginstellingen, screening van de gemeenschap bij uitbraken en quarantaine in havens/aan de grens.
-Denguevirus NS1-antigeensneltest: Detecteert vroege infectie (1-3 dagen na het begin van de symptomen) met resultaten binnen 15 minuten voor snelle triage.
- Denguevirus IgM/IgG-antilichaamtest: Maakt onderscheid tussen primaire en secundaire infecties om het risico op ernstige ziekte te beoordelen.
-Denguevirus NS1-antigeen + IgM/IgG gecombineerde sneltest: detecteert gelijktijdig antigeen en antilichamen voor een volledige diagnose.
-Chikungunya-virus IgM/IgG-antilichaamtest: Maakt differentiële diagnose met dengue mogelijk om ziekteverwekkers nauwkeurig te identificeren.
4.2 Scenario 2: Nauwkeurige diagnose en noodhulp
-Denguevirus I/II/III/IV nucleïnezuurdetectiekit: Detecteert en onderscheidt 4 serotypes (detectielimiet 500 kopieën/ml) voor het traceren van uitbraken.
- Gevriesdroogde denguevirus-PCR-kit: Transporteerbaar bij kamertemperatuur, geschikt voor gebieden met beperkte middelen en plotselinge uitbraken.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Detecteert gelijktijdig 3 arbovirussen voor een efficiënte differentiële diagnose bij complexe uitbraken.

Alle bovengenoemde reagentia zijn compatibel met het AIO 800 volledig geautomatiseerde systeem voor monsterverwerking en analyse, waardoor handmatige handelingen en kruisbesmetting worden verminderd en de efficiëntie en bioveiligheid worden verbeterd.
4.3 Scenario 3: Genomische surveillance en analyse van virale afstammingslijnen
Van toepassing op nationale referentielaboratoria en onderzoeksinstellingen voor volksgezondheid, in lijn met de positionering van NGS door de WHO.
De oplossingen voor genomische surveillance van Macro & Micro-Test ondersteunen sequencing van het volledige genoom voor het traceren van virussen, het ophelderen van transmissieketens, het monitoren van varianten en het aanpassen van vaccinatiestrategieën. Ze ondersteunen handmatige/geautomatiseerde workflows, verbeteren de doorvoer en reproduceerbaarheid en stellen laboratoria in staat om over te stappen van routinetesten naar geavanceerde surveillance, in lijn met de nadruk van de WHO op het versterken van de monitoring van virale evolutie.

4.4 Waarde van geïntegreerde oplossingen
Macro & Micro-Test biedt complete diagnostische oplossingen voor de detectie van arbovirussen, ter ondersteuning van elke fase van de bestrijding van uitbraken: snelle screeningsinstrumenten voor de eerstelijnsgezondheidszorg, moleculaire bevestiging voor een nauwkeurige diagnose en mogelijkheden voor analyse van het volledige genoom voor epidemiologische surveillance. Met hoogwaardige testen, flexibele workflows en automatiseringsklare platforms stellen deze oplossingen laboratoria en volksgezondheidssystemen in staat hun paraatheid en respons op opkomende arbovirale dreigingen wereldwijd te versterken.
Referenties
[1] Wereldgezondheidsorganisatie. Laboratoriumtesten voor het denguevirus: voorlopige richtlijnen, april 2025. Genève: Wereldgezondheidsorganisatie; 2025.
[2] WHO Global Arbovirus Initiative Technical Advisory Group. Strengthening Global Preparedness and Response to Arboviral Disease Threats: A Call to Action. Lancet Infect Dis. 2026;26(1):15-17.
[3] The Lancet Microbe. Het dilemma van dengue-diagnostiek overwinnen. Lancet Microbe. 2025;6(7):101190.
Geplaatst op: 20-03-2026
